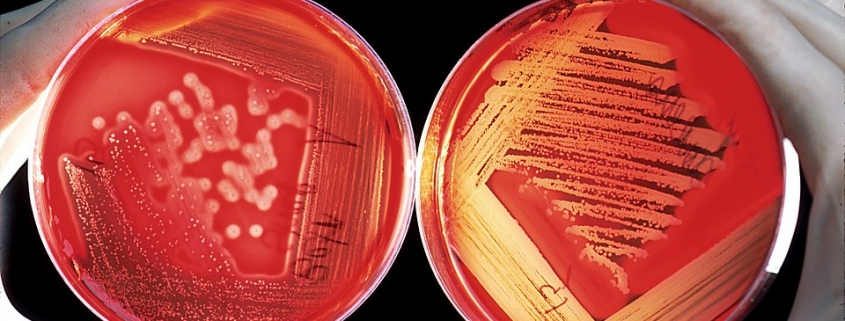
Ya encontramos los efectos del uso excesivo de antibióticos incluso en la Antártida. Investigadores han detectado en el suelo de la Antártida cientos de genes de resistencia diferentes. Estos genes confieren a las bacterias resistencia a los antibióticos. Incluso se detectó el supergen blaNDM-1, que se identificó hace algunos años en la India. Esto muestra lo rápido que se propagan las resistencias en todo el mundo.
Los antibióticos pierden eficacia, ya que en todo el mundo se están propagando gérmenes multirresistentes, inmunes a varias clases de antibióticos. Estos gérmenes multirresistentes ya no se encuentran solo en humanos y animales, sino también en suelos y aguas.
Especialmente peligroso es el “supergermen” multirresistente, la cepa NDM-1.
Esta cepa se descubrió en la India hace algunos años y es inmune a todas las clases habituales de antibióticos y a los antibióticos de emergencia del grupo de los carbapenémicos. Esta resistencia está causada por el gen blaNDM-1.
Un grupo de investigación dirigido por David Graham, de la Newcastle University, analizó 40 muestras de suelo tomadas en 2013 a lo largo del Kongsfjord, en el noroeste de Spitsbergen. Incluso en este ecosistema intacto de la Tierra se encuentran ahora gérmenes multirresistentes.
Se hallaron 131 genes de resistencia diferentes. . “Estos genes confieren protección frente a nueve clases diferentes de antibióticos, entre ellas los aminoglucósidos, los macrólidos y los betalactámicos, que se utilizan para tratar muchas infecciones”, informa Graham.
También se encontró el supergen blaNDM-1.
Esto demuestra que los genes de resistencia a los antibióticos ya se han extendido incluso a los rincones más remotos de la Tierra. Esto muestra lo rápido y ampliamente que se han propagado las resistencias a los antibióticos.
Los investigadores sospechan que los genes de resistencia fueron introducidos en Spitsbergen principalmente por aves. (Environment International, 2019)
Fuente: Newcastle University