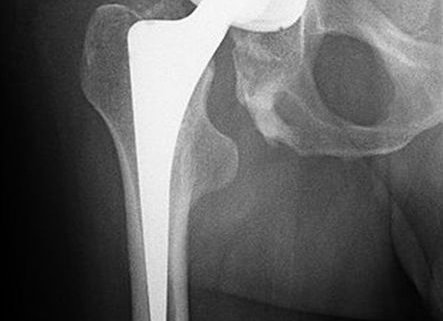
Bacteriofaagtherapie bij een chronische MRSA-gewrichtsprothese-infectie
Dit betreft de casus van een 72-jarige man met een chronische methicilline-resistente Staphylococcus aureus-gewrichtsprothese-infectie. Na de derde intraveneuze dosis bacteriofaagtherapie leidde een ongebruikelijke, reversibele transaminitis tot het staken van de bacteriofaagtherapie. Desondanks was de behandeling succesvol en werd de ernstige chronische infectie van de patiënt uitgeroeid.
Volgens de bevindingen van dit onderzoeksteam is dit de eerste casus van een bacteriofaagtherapie die succesvol is ingezet als adjuvante therapie voor de genezing van een chronische MRSA-PJI. Er is melding gemaakt van twee andere succesvolle bacteriofaagbehandelingen van MSSA en Pseudomonas PJI [10,11]. Uniek aan onze casus is dat er geen chronische suppressieve antibiotica werden gebruikt. Er is weinig bekend over de optimale behandelingsduur of de toedieningswegen bij PJI. Het plan was om langer te behandelen, maar de therapie werd gestopt toen er een significante transaminitis optrad. Desondanks werd een succesvolle sterilisatie van het gewricht en het gedevitaliseerde bot van de patiënt bereikt met een IA- en een 3-daagse IV-bacteriofaagtherapie in combinatie met standaard IV-antibiotica gedurende 6 weken. Gezien het vermogen van bacteriofagen om zichzelf te vermenigvuldigen, zijn als aanvulling op chirurgisch debridement wellicht slechts enkele dagen bacteriofaagtherapie vereist. Klinische studies zijn noodzakelijk om een passende duur van de bacteriofaagtherapie onder deze omstandigheden te bepalen [10,11].
Tot nu toe was bij alle PJI-patiënten die succesvol met bacteriofagen zijn behandeld, chirurgisch debridement vereist [10,11]. Deze operatie maakt het handmatig wegboenen van de biofilm mogelijk, garandeert dat de prothese behouden kan blijven en maakt de instillatie van bacteriofagen direct op de biofilm mogelijk. De lokale dosering van bacteriofagen kan essentieel zijn voor het elimineren van biofilminfecties, maar er zijn slechts beperkte gegevens beschikbaar buiten casusverslagen [10,11,12]. Bij herhaalde IA-doses traden geen bijwerkingen op, wat mogelijk te wijten is aan een beperkte systemische absorptie. Toekomstige studies moeten worden uitgevoerd om geschikte toedieningswegen bij PJI te bepalen.
Het meest unieke aspect van onze casus was de transaminitis die optrad na de derde IV-dosis bacteriofagen. Deze leek te zijn veroorzaakt door de bacteriofaagtherapie. Er werd geen andere verstoring van de leverfunctie vastgesteld en de transaminitis was reversibel en niet levensbedreigend. Afbeelding 2 toont de leverfunctie tijdens het verloop van de bacteriofaagtherapie.
De patiënte had hepatomegalie, maar een niet-alcoholische vette leverziekte kon radiologisch niet worden aangetoond en de biopsie werd uitgesteld. Meer dan 99% van de IV-bacteriofaagtherapie wordt snel afgebroken door de lever en de milt [13,14,15]. De theorie van dit onderzoeksteam stelt dat de onderliggende steatose de levermacrofagen ertoe aanzette een gedisreguleerde lokale cytokine-reactie op te wekken wanneer zij werden geconfronteerd met een groot aantal bacteriofagen die hepatisch geklaard moesten worden. Deze lokale reactie zou kunnen hebben geleid tot ontstekingsveranderingen in de hepatocyten, wat resulteerde in een stijging van AST en ALT. Dit wordt ondersteund door studies die de rol van levermacrofagen bij steatose onderzoeken en door oudere studies naar de hepatische klaring van bacteriofagen [13,14,15]. Het is niet bekend of lichte tot matige verhogingen van de leverenzymwaarden vaker voorkomen na toediening van bacteriofagen. Bovendien is niet bekend of voortgezette IV-toediening van bacteriofagen de transaminitis zou hebben verergerd of tot aanpassing en herstel zou hebben geleid. Vooralsnog moeten intraveneus toegediende bacteriofagen bij patiënten met een onderliggende leverpathologie met voorzichtigheid worden gebruikt en moeten de leverenzymen nauwgezet worden gecontroleerd. Deze casus is beperkt, aangezien we de cytokine-reactie van onze patiënt op de bacteriofaagtherapie niet hebben onderzocht. Toekomstige studies zouden deze respons moeten evalueren om meer te weten te komen over de normale menselijke cytokine-respons op bacteriofaagtherapie.
Samenvattend kan worden gesteld dat behoud van de prothese van de patiënt vanwege ernstige boterosie niet mogelijk was. We waren echter in staat om de ernstige chronische MRSA-PJI van de patiënt te steriliseren met een enkele virulente bacteriofaag, die gedurende drie dagen IA en IV werd toegediend in combinatie met IV-antibiotica. Er zijn meer PJI-studies nodig om de optimale duur en wijze van toediening van de fagen vast te stellen. Bacteriofaagtherapie heeft een enorm potentieel voor de genezing van PJI, maar er moeten klinische fase 1- en 2-studies worden uitgevoerd.
Vertaald uit de bron:
https://www.mdpi.com/2079-6382/9/5/241/htm
Salvage Bacteriophage Therapy for a Chronic MRSA Prosthetic Joint Infection
door James B. Doub,*, Vincent Y. Ng, Aaron J. Johnson, Magdalena Slomka, Joseph Fackler, Bri’Anna Horne, Michael J. Brownstein, Matthew Henry,