Dit gen maakt salmonella resistent tegen alle antibiotica
“Antibiotica waren ongetwijfeld een van de belangrijkste medische ontwikkelingen van de 20e eeuw. Tegelijkertijd groeien ze echter uit tot een van de grote uitdagingen van de 21e eeuw. Dankzij een zeer soepel voorschrijfbeleid bij menselijke patiënten en een extensief gebruik van antibiotica in de veeteelt, verspreiden zogenaamde multiresistente bacteriën zich inmiddels wereldwijd – vooral in de medisch uitstekend verzorgde industrielanden. Het gaat hierbij om ziekteverwekkers die immuun zijn voor veel antibiotica. In de VS is nu voor het eerst een bacterieel gen gevonden dat resistentie verleent tegen de zogenaamde ‘last resort’-antibiotica, oftewel tegen de meest effectieve en sterkste bestaande antibiotica.
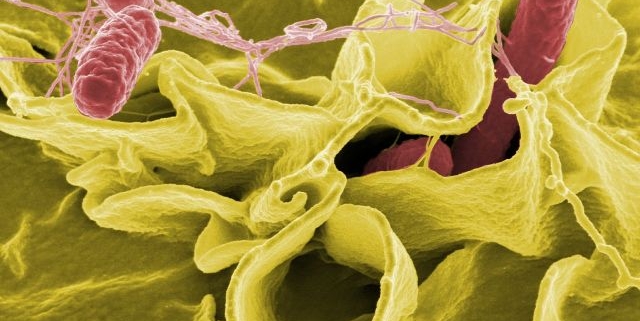
Salmonella zijn bacteriën die geassocieerd worden met voedselvergiftigingen. In de regel is een salmonellainfectie een kwestie van geduld – op een gegeven moment verdwijnt deze weer. Niet gevaarlijk, maar wel onaangenaam. Dit ligt anders bij bijzonder jonge of oude mensen, evenals bij mensen met een verzwakt immuunsysteem. Voor hen kunnen salmonellainfecties een risico vormen, waardoor er vaak antibiotica worden voorgeschreven.
En hier stuiten we op een probleem: net als veel andere bacteriën heeft ook salmonella een resistentie ontwikkeld tegen de meeste antibiotica. Meer specifiek tegen vrijwel alles behalve colistine, een antibioticum dat nu als laatste medicamenteuze behandelingsmogelijkheid voor salmonellainfecties wordt beschouwd. En nu ziet het ernaar uit dat ook dit medicijn niet lang meer zal werken. Onderzoekers in de VS hebben een gen ontdekt dat salmonella het vermogen geeft om zich tegen colistine te weren. De bacterie is daarmee nagenoeg niet meer met antibiotica te behandelen.
Gen komt uit China
Het gen staat bekend als mcr-3.1 en stond al jaren op de watchlist van veel wetenschappers. Nu lijkt het voor het eerst in de VS te zijn opgedoken.
„Public health officials have known about this gene for some time. In 2015, they saw that mcr-3.1 had moved from a chromosome to a plasmid in China, which paves the way for the gene to be transmitted between organisms. For example, E. coli and Salmonella are in the same family, so once the gene is on a plasmid, that plasmid could move between the bacteria and they could transmit this gene to each other. Once mcr-3.1 jumped to the plasmid, it spread to 30 different countries, although not – as far as we knew – to the US„, aldus Siddhartha Thakur, een van de auteurs van de studie.
Het gen werd ontdekt tijdens routineonderzoeken die bedoeld waren om nieuwe multiresistente bacteriestammen op te sporen. Het mcr-3.1-gen werd aangetroffen in een ontlastingsmonster dat al in 2014 was afgenomen van een patiënt die in China een salmonellainfectie had opgelopen. In theorie is het gen in staat om over te gaan op de aanzienlijk gevaarlijkere E. coli-bacterie.
De verspreiding van dit gen is een volgende stap in de richting van superresistente bacteriën. Er worden echter voortdurend nieuwe antibiotica ontwikkeld en er wordt ook onderzoek gedaan naar andere behandelmethoden voor multiresistente bacteriën.”
Bron: https://www.trendsderzukunft.de/medizin-dieses-gen-laesst-salmonellen-resistent-gegen-alle-antibiotika-werden/amp/