Gemini hat gesagt
Meta-Description: Entdecken Sie die Macht der Bakteriophagen: Wie die Phagen-Antibiotika-Synergie (PAS) multiresistente Keime besiegt und die Medizin revolutioniert. Jetzt lesen!
Die Macht der Bakteriophagen: Ein neuer Horizont im Kampf gegen die Antibiotikaresistenz
Die Geschichte der Medizin ist geprägt von Triumphen über unsichtbare Feinde. Doch der größte Sieg des 20. Jahrhunderts – die Entdeckung der Antibiotika – droht im 21. Jahrhundert zu einer gefährlichen Sackgasse zu werden. Während herkömmliche Medikamente gegen „Supererreger“ versagen, rückt eine winzige, hochspezialisierte Entität in den Fokus, die bereits seit Jahrmilliarden auf unserem Planeten existiert: der Bakteriophage.
In diesem Artikel beleuchten wir die Erkenntnisse der aktuellen Forschung zur Macht der Bakteriophagen und untersuchen, warum die Kombination aus Biologie und Chemie unsere letzte Verteidigungslinie sein könnte.
Zusammenfassung: Key Takeaways
-
Präzisionsangriff: Bakteriophagen töten spezifische Krankheitserreger, ohne das nützliche Mikrobiom (z. B. im Darm) zu schädigen.
-
PAS-Effekt: Die Phagen-Antibiotika-Synergie verstärkt die Wirkung herkömmlicher Medikamente um ein Vielfaches.
-
Resistenz-Umkehr: Phagen können Bakterien dazu zwingen, ihre Antibiotikaresistenz aufzugeben, um zu überleben.
-
Biofilm-Killer: Phagen dringen in bakterielle Schutzschichten ein, an denen Antibiotika scheitern.
-
Individuelle Medizin: Die Therapie wird mittels Phagogramm exakt auf den Patienten zugeschnitten.
1. Das Ende des Antibiotika-Zeitalters? Die globale Krise
Wir leben in einer Ära, in der routinemäßige Operationen, Krebsbehandlungen oder einfache Infektionen wieder lebensbedrohlich werden könnten. Die WHO stuft die Antibiotikaresistenz als eine der zehn größten globalen Bedrohungen für die öffentliche Gesundheit ein.
Warum versagen Antibiotika?
Antibiotika wirken meist durch chemische Blockaden. Sie hemmen den Aufbau der Zellwand oder stören die Eiweißproduktion der Bakterien. Bakterien reagieren darauf mit evolutionärer Anpassung: Sie entwickeln Enzyme, die das Antibiotikum zerstören, oder „Pumpen“ (Efflux-Pumpen), die den Wirkstoff aus der Zelle schleusen. Da Bakterien sich alle 20 Minuten teilen können, verbreiten sich diese Resistenzen rasant.
Die Notwendigkeit für Antibiotikaresistenz Lösungen
Die pharmazeutische Pipeline für neue Antibiotika ist nahezu ausgetrocknet. Es ist ökonomisch und wissenschaftlich schwierig, ständig neue Wirkstoffe zu finden, die nicht sofort wieder durch Resistenzen unwirksam werden. Hier tritt die Bakteriophagen Therapie auf den Plan – nicht als statisches Medikament, sondern als lernfähiger, biologischer Jäger.
2. Bakteriophagen: Die Biologie der „Bakterienfresser“
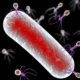
Bakteriophagen (kurz Phagen) sind Viren, die ausschließlich Bakterien infizieren. Sie sind so zahlreich, dass man schätzt, dass es Phagen auf der Erde gibt – eine Zahl mit 31 Nullen.
Der lytische Zyklus: Präzision auf molekularer Ebene
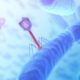
Ein Phage ist wie eine hochmoderne Drohne. Er erkennt sein Zielbakterium anhand spezifischer Rezeptoren auf dessen Oberfläche. Passt der Phage nicht exakt zum Bakterium, passiert gar nichts – das ist der Grund, warum sie für menschliche Zellen absolut harmlos sind.
Sobald der Phage andockt, injiziert er seine DNA. Die Bakterienzelle wird umfunktioniert und produziert hunderte neuer Phagen. Schließlich platzt das Bakterium (Lyse) und setzt die „Armee“ frei, die den nächsten Erreger angreift. Dieser Prozess setzt sich so lange fort, wie die spezifischen schädlichen Bakterien vorhanden sind.
3. Wissenschaftlicher Fokus: Die Phagen-Antibiotika-Synergie (PAS)
Das eigentliche Geheimnis hinter der Macht der Bakteriophagen liegt in ihrer Zusammenarbeit mit der klassischen Medizin. Die Phagen-Antibiotika-Synergie (PAS) beschreibt das Phänomen, bei dem die Kombination beider Therapien effektiver ist als die Summe ihrer Einzelteile.
Wie funktioniert PAS im Detail?
Wissenschaftliche Studien, wie auf phage.help beschrieben, zeigen faszinierende Mechanismen:
-
Stress-Induktion: Wenn ein Bakterium mit einer geringen Dosis eines Antibiotikums (z. B. einem Beta-Laktam) konfrontiert wird, gerät es unter Stress. In diesem Zustand vergrößert es oft seine Zelloberfläche (Filamentierung). Diese größere Oberfläche bietet dem Phagen mehr „Landeplätze“ für seine Rezeptoren, was die Infektionsrate massiv steigert.
-
Die evolutionäre Zwickmühle: Dies ist der entscheidende strategische Vorteil. Will das Bakterium gegen den Phagen resistent werden, muss es oft seine Oberflächenstruktur verändern – genau jene Strukturen, die es für die Antibiotikaresistenz benötigt. Das Bakterium muss sich entscheiden: „Werde ich resistent gegen den Phagen oder behalte ich meine Resistenz gegen das Antibiotikum?“. Beides gleichzeitig ist biologisch oft zu „teuer“ für den Keim.
-
Wiederherstellung der Sensitivität: In vielen Fällen führt der Druck durch die Phagen dazu, dass Bakterien wieder empfindlich für Antibiotika werden, gegen die sie zuvor jahrelang immun waren.
4. Exkurs: Die Rückkehr eines vergessenen Wissens (Georgien & Osteuropa)
Während die westliche Welt nach 1945 fast ausschließlich auf Antibiotika setzte, blieb die Phagenforschung im Ostblock, insbesondere in Georgien, lebendig. Das Eliava-Institut in Tiflis ist heute das weltweit führende Zentrum für klinische Phagenanwendungen.
Warum Georgien uns voraus ist
In Georgien werden Phagen-Cocktails seit fast 100 Jahren zur Behandlung von Magen-Darm-Infektionen, Verbrennungen und eiternden Wunden eingesetzt. Während wir im Westen Phagen als „neue Technologie“ betrachten, sind sie dort ein bewährter Bestandteil des öffentlichen Gesundheitssystems. Die aktuelle Forschung nutzt diesen Erfahrungsschatz nun, um standardisierte Protokolle für die moderne Bakteriophagen Therapie im Westen zu entwickeln.
5. Biofilme: Die uneinnehmbare Festung knacken
Ein Hauptgrund für chronische Infektionen (z. B. bei Implantaten, in der Lunge bei Mukoviszidose oder bei diabetischen Wunden) ist der Biofilm. Dies ist eine zähe Schleimschicht, in der sich Bakterien verschanzen. Antibiotika kommen hier oft nicht durch.
Phagen besitzen jedoch spezielle Enzyme, sogenannte Depolymerasen. Diese wirken wie chemische Scheren, die den Biofilm zerschneiden. Sobald die schützende Schicht aufgebrochen ist, können sowohl die Phagen als auch die begleitenden Antibiotika die Bakterien im Inneren erreichen und eliminieren.
6. Das Phagogramm: Personalisierung statt „Gießkanne“
Ein zentraler Pfeiler der modernen Phagentherapie ist das Phagogramm. Ähnlich wie ein Antibiogramm ermittelt es im Labor, welche spezifischen Phagen aus einer Biobank gegen den individuellen Bakterienstamm eines Patienten wirken.
Dieser Ansatz der personalisierten Medizin verhindert die Zerstörung der gesunden Flora. Während ein Antibiotikum oft wie ein „Waldbrand“ wirkt, der alles vernichtet, agiert die Phagentherapie wie ein „Scharfschütze“, der nur das Ziel ausschaltet.
7. FAQ – Häufig gestellte Fragen
1. Sind Bakteriophagen sicher für Menschen? Ja. Da Phagen hochspezifisch auf bakterielle Oberflächenrezeptoren angewiesen sind, können sie menschliche Zellen weder infizieren noch schädigen. Es gibt keine bekannten toxischen Wirkungen auf den menschlichen Organismus.
2. Kann man Phagen und Antibiotika gleichzeitig einnehmen? Ja, das ist oft sogar das Ziel. Die Phagen-Antibiotika-Synergie zeigt, dass die Kombination die Heilungschancen bei multiresistenten Keimen signifikant erhöht. Die genaue Abstimmung sollte jedoch durch spezialisierte Ärzte erfolgen.
3. Warum ist die Therapie in Deutschland noch nicht Standard? Das Hauptproblem liegt in der Zulassung. Da Phagen biologisch aktiv sind und sich verändern, passen sie nicht in das starre europäische Arzneimittelrecht für chemische Medikamente. In Deutschland ist die Behandlung meist nur als „individueller Heilversuch“ möglich.
4. Woher bekommt man die passenden Phagen? Spezialisierte Institute (z. B. in Polen, Belgien oder Georgien) verfügen über große Phagen-Banken. Dort werden Patientenproben getestet und passende Phagen-Cocktails zusammengestellt. Weitere Infos finden Sie auf der Behandlungsseite von phage.help.
5. Helfen Phagen auch bei „schlafenden“ Bakterien? Manche Phagen können auch sogenannte Persister-Zellen infizieren, die sich im Ruhezustand befinden und von Antibiotika ignoriert werden. Sobald diese Bakterien wieder aktiv werden, schlägt der Phage zu.
Fazit: Die Macht der Biologie nutzen
Die Studie zur Macht der Bakteriophagen unterstreicht, dass wir den Kampf gegen multiresistente Erreger nicht allein mit Chemie gewinnen werden. Wir müssen lernen, mit den natürlichen Feinden der Bakterien zusammenzuarbeiten. Die Phagen-Antibiotika-Synergie (PAS) bietet nicht nur eine Lösung für verzweifelte Patienten, sondern stellt einen Paradigmenwechsel in der gesamten Medizin dar.
Es ist an der Zeit, dass wir das Potenzial dieser winzigen „Bakterienfresser“ voll ausschöpfen und die regulatorischen Hürden überwinden, um diese lebensrettende Therapie jedem zugänglich zu machen.
Interessante interne Links für Sie:
Hinweis: Dieser Blogbeitrag dient der allgemeinen Information und ersetzt keine ärztliche Diagnose oder Therapieempfehlung. Bei gesundheitlichen Beschwerden wenden Sie sich bitte an einen spezialisierten Mediziner.
Autor: David Brand
David Brand widmet sich als Autor der fundierten Aufklärung über Gesundheitsthemen. Sein Ziel ist es, verlässliche Informationen in den Fokus zu rücken und Patienten dabei zu helfen, komplexe medizinische Sachverhalte besser einordnen zu können. Durch gründliche Recherche und eine klare Sprache schafft er Orientierung im modernen Gesundheitsdschungel – stets mit Fokus auf geprüfte Fakten.